Efecto de la nutrición sobre la mortalidad embrionaria en bovinos
Rómulo Campos G. MV., DSc. Érika A. Hernández, Est. Zootecnia
En este enlace encontraras los efectos de la nutrición sobre todos los aspectos reproductivos Como la nutrición mejora la fertilidad del bovino
La mortalidad embrionaria (ME), es un trastorno reproductivo responsable por cerca del 15% de las fallas de la gestación. En sí, la mortalidad embrionaria puede dividirse en dos grandes grupos, ME temprana aquella que sucede en los primeros días de la gestación, por problemas específicos de reconocimiento materno-fetal, que no generan alteración significativa del ciclo estral, ya que, no se afecta el cuerpo lúteo (Bondurant, 2004). Leer mas sobre el aborto en bovinos
La segunda forma de la mortalidad embrionaria, denominada ME tardía, altera el ciclo estral y se presenta por rechazo de la implantación en sus primeras fases, usualmente se presenta entre el día 25 y 40 post servicio. Según Geary (2005) existen múltiples causas asociadas a la mortalidad embrionaria, entre estas causas se listan problemas de rechazo inmunológico, ausencia de factores de reconocimiento materno-fetal, problemas infecciosos, estrés y deficiencias nutricionales, entre estas últimas se podrían citar:
Te puede interesar Efecto de la nutrición sobre la retención de placenta en bovino.
Deficiencia de beta carotenos y la muerte embionaria
Los betacarotenos son precursores de la vitamina A (provitamina A). Son pigmentos vegetales de color amarillo o naranja que, una vez ingeridos, se transforman en el hígado y en el intestino delgado en vitamina A. Son antioxidantes que ayudan al organismo a eliminar los radicales libres tóxicos que causan la oxidación de los tejidos (reacción química de peroxidación que produce lesión en los tejidos ya que los peróxidos son compuestos tóxicos y cancerígenos) en células, proteínas y material genético como DNA.
Los radicales libres se forman normalmente como subproductos del metabolismo oxidativo energético del organismo. Los betacarotenos actúan atrapando estos radicales libres y moléculas de oxígeno libre y de ahí su efecto protector el cual se centra en la defensa de la pared epitelial, pues al ser precursores de la vitamina A, induciendo su síntesis protegen la pared epitelial del debilitamiento de sus membranas, evitando así, la fácil entrada de microorganismos patógenos que puedan, específicamente en el caso de una hembra gestante producir infecciones que ataquen al embrión originando la muerte de éste, ya que aumenta la resistencia inmunológica.
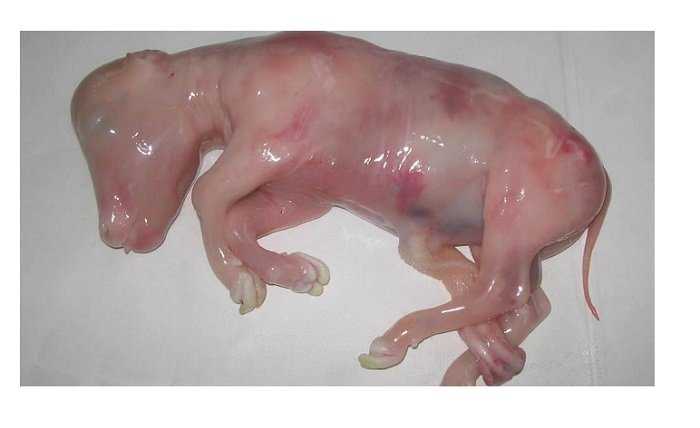
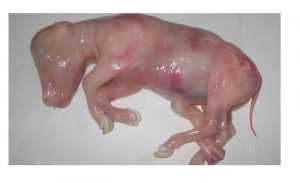
Además, también intervienen en la diferenciación de las células madre del embrión, evitando que ocurran malformaciones que puedan originar mortalidad embrionaria, y también evitando la asimetría del organismo que se esta formando.
La vitamina A, ayuda en la conservación de los epitelios para un funcionamiento normal. Una deficiencia de ésta, produce una alteración de los epitelios que revisten el aparato genital, pudiendo ocasionar disminución de la barrera protectora que forman las membranas, los microorganismos patógenos pueden entrar fácilmente, desencadenando la muerte del embrión.
La vitamina A, actúa en el momento en que las células madre del embrión entran en una zona de éste, llamada “Nódulo de Hensen”, comienzan a formar tres capas embrionales de células que dan paso al sistema nervioso, digestivo, circulatorio y otros sistemas del cuerpo. Células específicas ubicadas en esta zona del embrión utilizan sus cilios (que segregan vitamina A para crear corrientes en el fluido que las rodea y dirigir a las células madre hacia su destino final.
Estas células madre, antes de llegar al nódulo del embrión “no están orientadas espacialmente y tampoco están diferenciadas en tejidos concretos” aunque luego de cruzar esta puerta, reciben ordenes genéticas necesarias para colocarse en el interior del organismo en desarrollo y conocer cuál va a se su diferenciación especifica. Entonces la acción de esta vitamina hace que algunas de estas células ignoren las instrucciones de diferenciación izquierda y derecha, prosiguiendo simétricamente.
Según esto, en una deficiencia de vitamina A, el aspecto exterior del cuerpo también acabaría por ser asimétrico perdiendo potencial de aceptación en la implantación, llevando a los mecanismos naturales de vigilancia de estabilidad celular a su destrucción y por tanto generando mortalidad embrionaria (Torres et al. 2002).
Proteína y muerte embionaria
El exceso de proteína cruda en la dieta ha sido asociado con mortalidad embrionaria. Hay una hipótesis que plantea que la concentración de LH, y por lo tanto de progesterona, podrían verse afectadas por elevados niveles de proteína en la ración, tal vez no en forma directa sino, por la deficiencia de energía que los excesos proteicos generan.
Existe una relación estrecha entre el exceso de proteína cruda con la concentración de progesterona, esta relación es a través de una “exacerbación” del balance energético negativo en vacas al comienzo de la lactación, por el gasto de precursores de la glucosa y el consumo energético extra que supone transformar el amonio en urea (este hecho sólo se relaciona con la proteína degradable en rumen).
Esto ocasionaría aumento del balance energético negativo y caída de la glicemia, lo que sería captado por la hipófisis como una señal negativa para la liberación de LH.
Un exceso de proteína tal que reduzca los niveles de progesterona y de bTP-1 proteína trofoblástica, hoy día, identificada como el Interferón tau (IFN-t), perteneciente a una subclase de los interferones Omega, y definidos como los factores de reconocimiento materno-fetal en bovinos, podría ocasionar mortalidad embrionaria en torno al día 17 después de la inseminación debido a la pérdida del efecto de ambos compuestos frente a la respuesta inmunitaria de la madre. (Martínez, et al. 1999; Moreira, et al.2001)
Niveles excesivos de proteína en la dieta que conduzcan a altos niveles de urea en la sangre, reducen el pH uterino con lo que se estimula la producción de la prostaglandina F2 alfa (PGF2-α) la que, a su vez estimula la contractibilidad uterina y reduce la viabilidad de implantación del embrión (Correa, 2001).
Así mismo, se ha observado que altas concentraciones de urea en sangre reducen la formación de progesterona, en ambos casos se altera la actividad reproductiva.
La progesterona es una hormona lipídica que es producida por el cuerpo lúteo bajo el estímulo del (IGF-I)) y, como se había señalado previamente, se ha observado que este factor de crecimiento también se ha reducido en la medida en que se ha incrementado el potencial genético para producción de leche de tal manera que la reducción en la concentración del IGF–I podría ser una de las causas de la disminución en la concentración de la progesterona. Ahora, aunque es considerado que la hormona del crecimiento (HC) regula la síntesis de IGF–I en el hígado, esta hormona no es efectiva a menos que exista un nivel umbral de insulina y esta última también se ve reducida en vacas de alta producción al inicio de la lactancia (Correa, 2001) y bajo condiciones de balance energético negativo, tal como se presenta en el postparto temprano.